La mole et la quantité de matière – Cours Physique-Chimie Tronc Commun (TCS BIOF)
🧪 Introduction à la mole et à la quantité de matière
Tu as sûrement déjà entendu parler de la “mole” en cours de physique-chimie tronc commun, mais cette notion reste floue pour beaucoup d’élèves. Pourtant, elle est essentielle pour comprendre la chimie moderne, notamment dans le programme du tronc commun scientifique au Maroc. Dans cet article, on va t’expliquer de façon claire, simple et scientifique ce qu’est la mole, comment elle se calcule, et pourquoi elle est si importante.
✅ Qu’est-ce que la mole ?
La mole est une unité de mesure qui permet de compter les entités microscopiques comme les atomes, molécules, ou ions.
📌 1 mole = 6,02 × 10²³ entités, ce nombre est appelé constante d’Avogadro (Na).
👉 Par exemple, si tu as 1 mole d’atomes de carbone, cela veut dire que tu possèdes 6,02 × 10²³ atomes de carbone, et leur masse totale est de 12 g.
🧮 Calcul de la quantité de matière
1️⃣ Relation entre le nombre d’entités et la quantité de matière
n = N / Na- N : nombre d’entités
- Na : constante d’Avogadro = 6,02 × 10²³ mol⁻¹
2️⃣ Relation entre la masse et la quantité de matière
n = m / M- m : masse en grammes (g)
- M : masse molaire en g/mol
⚖️ Masse molaire : Définition et exemples
La masse molaire (M) est la masse d’une mole d’une substance, exprimée en g/mol.
🔹 Exemples de masses molaires atomiques :
- H : 1,0 g/mol
- O : 16,0 g/mol
- C : 12,0 g/mol
- N : 14,0 g/mol
🔹 Calcul de masse molaire moléculaire
Exemple : Eau (H₂O)
M(H₂O) = 2 × M(H) + M(O) = 2 × 1,0 + 16,0 = 18,0 g/mol💨 Volume molaire des gaz
📐 Loi d’Avogadro – Volume molaire
Dans les mêmes conditions de température et de pression, tous les gaz occupent le même volume molaire :
- À 0 °C et 1 atm → Vm = 22,4 L/mol
- À 20 °C → Vm = 24,0 L/mol
n = V / Vm⚖️ Densité des gaz
La densité (notée d) est le rapport entre la masse d’un volume de gaz et celle du même volume d’air :
d = M_gaz / M_airoù M_air ≈ 29 g/mol
🔹 Exemple : Méthane CH₄
M(CH₄) = 12 + 4 × 1 = 16 g/mol
d = 16 / 29 ≈ 0,55Pour plus d’exercices et fiches du cours sur la mole clic sur ce lien:
Cours+ exercices “La mole et quantité de matière”
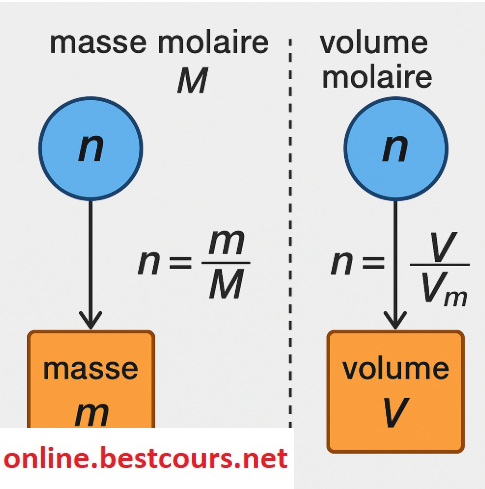
📊 Schéma Résumé “la mole”
Voici un schéma visuel pour mieux comprendre les relations :
🧠 Conclusion
La mole est une notion essentielle en physique-chimie. Grâce à elle, tu peux faire le lien entre nombre d’entités, masse et volume. Ce cours t’aide à maîtriser les bases de quantite de matiere programme de TCS BIOF.
🧪 Exercices la quantité de matiére (la mole)!
📚 aller loin: la mole et la quantite de mataire tronc commun
- CNRS – www.cnrs.fr
- Université de Strasbourg – www.unistra.fr
- Programme marocain officiel – Physique-Chimie Tronc Commun
- Document pédagogique : “La mole et les grandeurs molaires”
- cours et exercices “La Mole” tronc commun